Wir nehmen Datenschutz ernst!
Unsere Seiten nutzen in der Grundeinstellung nur technisch-notwendige Cookies. Inhalte Dritter (YouTube und Google Maps) binden wir erst nach Zustimmung ein.
Cookie-Einstellungen | Impressum & Datenschutz
CRISPR - Eine neue Technologie

Mit neuen gentechnischen Verfahren wie CRISPR/Cas können Wissenschaftler in bisher ungeahntem Ausmaß in die DNA, also das Erbgut von Mikroorganismen, Pflanzen, Tieren und Menschen eingreifen.
Mit diesem Verfahren sind Chancen und Risiken verbunden. Um diese bewerten zu können, ist es wichtig zu wissen, wie zuverlässig diese Verfahren arbeiten und welche Unwägbarkeiten mit ihnen verbunden sind. Daraus ergibt sich, wie ihre Anwendung geregelt werden sollte. Doch zuallererst kommt es darauf an, ihre Funktionsweise zu verstehen.
So funktioniert CRISPR
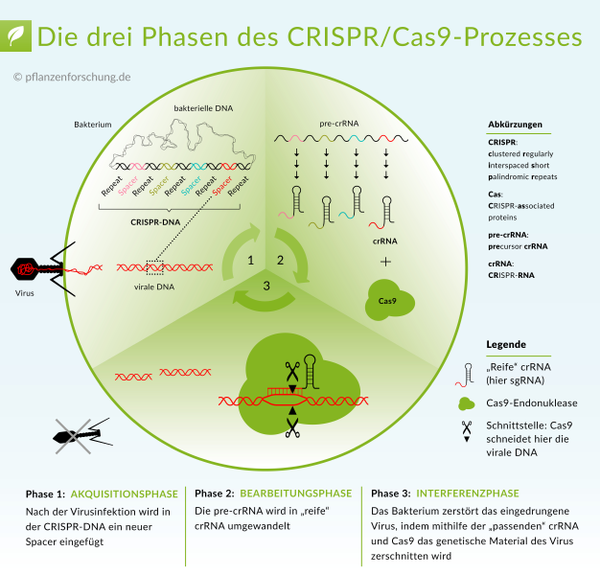
CRISPR steht für Clustered Regularly Interspaced Short Palindromic Repeats, zu deutsch etwa kurze, regelmäßige Abschnitte sich wiederholender DNA. Diese Abschnitte fanden Wissenschaftler bereits 1987 im Erbgut zahlreicher Bakterien. Doch erst 20 Jahre später konnten Forscher ihre Funktion erklären: Wenn Viren in die Zelle eindringen, baut das Bakterium einen Teil der fremden DNA in das eigene Erbgut ein. Es dient dort dem Immunsystem als eine Art Zettelkasten. Greifen die Viren erneut an, kann die Zelle sie anhand der abgespeicherten DNA-Sequenzen identifizieren. Zerstört werden sie dann durch ein passendes Enzym, das die eingedrungene DNA zerschneiden kann. Die bekannteste dieser Gen-Scheren heißt Cas9, andere werden als Cpf1 oder C2c2 bezeichnet.
CRISPR ist also eine Erfindung der Natur. 2012 erkannten Emmanuelle Charpentier und Jennifer Doudna an der University of Berkeley den grundlegenden Mechanismus der Gentechnik-Schere und demonstrierten, wie sich damit das Erbgut von Bakterien verändern ließ. Eine Arbeitsgruppe um Feng Zhang vom Broad Institute in Cambridge zeigte ein Jahr später, wie sich die Methode bei Pflanzen, Tieren und Menschen anwenden lässt.
CRISPR als neues gentechnisches Verfahren
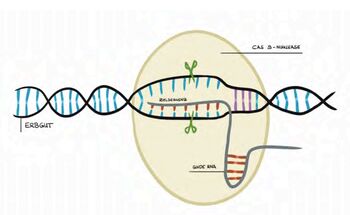
Das geht im Prinzip so: Eine gentechnisch hergestellte CRISPR-Komponente, die Gen-Sonde, wird mit dem Enzym Cas9 (oder einer verwandten Gen-Schere) gekoppelt. Die Gen-Sonde führt das Enzym zu einer bestimmten Stelle im Erbgut – das kann in Zellen von Pflanzen, Mikroorganismen, Tieren oder Menschen geschehen. Dort trennt die Gen-Schere den DNA-Strang. Die Zelle repariert diese Stelle, wodurch Veränderungen entstehen. Die als SDN-1 (site directed nuclease-1) bezeichnete Technik erzeugt an einem ausgewählten Ort zufällige kleine Änderungen, die nur wenige Basenpaare der DNA betreffen. Sie wird häufig genutzt, um eine spezifische Funktion von Genen abzuschalten. Bei der SDN-2 Technik werden kleine, im Labor gefertigte DNA-Stücke als Reparatur-Vorlagen an den Schnitt transportiert und bei der Reparatur mit eingebaut. Damit lässt sich das Erbgut an dieser Stelle gezielt ändern. SDN-3 bezeichnet Verfahren, bei denen größerer DNA-Stücke, etwa ganze Genabschnitte, eingeschleust und eingebaut werden.
Damit das CRIPR-Cas System überhaupt in die Zelle gelangt, gibt es zwei Möglichkeiten, die auch bei den alten gentechnischen Eingriffen genutzt werden: Das Bodenbakterium Agrobacterium tumefaciens infiziert die Zielpflanze und überträgt dabei die DNA des CRISPR/Cas-Systems in die Zelle. Oder die Zelle wird mit sehr kleinen Metallpartikeln beschossen, die mit der DNA des CRISPR/Cas-Systems beschichtet wurden (Gen-Kanone). In beiden Fällen baut die Zelle die DNA in ihr Erbgut ein und produziert das CRISPR/Cas-System, das dann seine Arbeit erledigt.
Unbegrenzte Möglichkeiten?

„Im Prinzip können wir mit dieser Technologie das Genom jeder Zelle und jedes Organismus umschreiben“, erklärte Emmanuelle Charpentier einmal in einem Interview die Möglichkeiten von CRISPR/Cas. Dabei funktioniert dieses Umschreiben, das Genome Editing, so einfach, dass in den USA Internetfirmen bereits Do-It-Yourself-Baukästen anbieten, mit denen das Erbgut von Organismen, etwa E. coli-Darmbakterien, verändert werden kann.
Bei der Anwendung am Menschen sind es vor allem die Möglichkeiten, Erbkrankheiten zu heilen und Krebs zu bekämpfen, die die Forscher beschäftigen - und zahlreiche ethische Fragen aufwerfen. Ethikrat: Eingriffe in die menschliche Keimbahn, Mai 2019
Bei Nutztieren konzentrieren sich die Anwendungen auf drei Bereiche:
- Die Tiere sollen mehr Ertrag liefern, etwa mehr Muskelfleisch ansetzen oder längere Wollhaare bekommen.
- Sie sollen besser an die Haltungsbedingungen angepasst werden, etwa durch genetische Hornlosigleit bei Rindern oder virusresistente Schweine.
- Ihre Erzeugnissse sollen für den Menschen gesünder werden, etwa allergenfreie Hühnereier.
Ausführlich in: Friends of Earth: Genetically engineered animals
Nutzpflanzen sollen mit CRISPR/Cas so gezüchtet werden, dass sie resistent gegen Krankheiten werden und mit stressigen Bedingungen wie Hitze, Trockenheit oder salzigen Böden besser zurechtkommen. Diese Ziele lassen sich nach Ansicht der Züchter mit den neuen gentechnischen Verfahren schneller erreichen als mit herkömmlicher Züchtung. Das ist aus deren Sicht besonders wichtig, da diese optimierten Pflanzen besser mit dem Klimawandel zurechtkämen und helfen würden, die Welternährung zu sichern.
Ein weiterer Forschungsschwerpunkt bei Pflanzen ist die Nährstoffzusammensetzung, etwa gesundheitsfördernde Fettsäuremuster bei Ölpflanzen oder das Wegzüchten von Allergenen.
Ebenfalls angewandt wird CRISPR/Cas, um die Produktion von Rohstoffen und Lebensmitteln zu vereinfachen, etwa durch herbizidresistente Pflanzen oder solche, die beim Anschneiden nicht bräunen.
Bei allen diesen Eingriffen gehen die Anwender davon aus, dass sie präzise und ohne Nebenwirkungen erfolgen. Die Eingriffe werden als Gen-Chirurgie bezeichnet oder als Umschreiben des Erbguts.
Beispielhaft findet sich diese Haltung auf der gentechnikfreundlichen Webseite von Transgen.
Von wegen präzise und sicher

Kritische Wissenschaftler bezweifeln, ob sich ein von Bakterien abgeschautes System so einfach über biologische Grenzen hinweg übertragen lässt. „Die Zellen von Pflanzen und Tieren sind anders aufgebaut als diejenigen von Bakterien (oder das Erbgut von Viren) und verfügen über andere Regulationsmechanismen. Die Folge könnten ungeahnte und unbeabsichtigte Änderungen der DNA sein“, schreibt etwa das Institut Testbiotech. Es argumentiert, dass die Natur vielfältige Regeln der Genregulierung hervorgebracht habe, die von der modernen Biowissenschaft bei weitem nicht verstanden würden.
Testbiotech: Synthetische Gentechnik und ihre Anwendung bei Pflanzen und Tieren in der Landwirtschaft
Deshalb kommt es auch bei Eingriffen mit CRISPR/Cas zu oft unerwarteten Effekten, Diese werden unterschieden in On-Target-Effekte, die am Ort des Eingriffs ins Erbgut auftreten und Off-Target-Effekte, die weiter entfernte Bereiche des Erbguts betreffen. Diese Effekte können zum Beispiel auftreten, weil die Gen-Scheren nicht so präzise schneiden wie angenommen, weil die Reparaturen ungeplante Ergebnisse bringen oder sich die Gene anders verhalten als geplant. Sie wurden inzwischen in einer Reihe von Veröffentlichungen beschrieben. Aktuelle Beispiele sind:
University of Delaware, ChristianaCare’s Gene Editinig Institute: New tool for rapid analysis of CRISPR reveals frequent, unintended DNA changes (10.12.2019)
Boris V. Skryabin et al: Pervasive head-to-tail insertions of DNA templates mask desired CRISPR-Cas9–mediated genome editing events (Science Advances, 12.02.2020)
Arne H. Smits, Frederik Ziebell et al: Biological Plasticity Rescues Target Activity in CRISPR Knockouts (16.11.2019)
Die Plattform GMWatch hat weitere einschlägige Studien aufgelistet.
Das Bundesamt für Naturschutz (BfN) betont, dass auch kleinste Abweichungen im Genom gravierende Auswirkungen haben können: „Auch einzelne Deletionen oder Insertionen, also das Einfügen oder Entfernen einzelner Buchstaben der DNA, können Organismen stark ändern. Bekannt ist dies bei Erbkrankheiten wie der Sichelzellenanämie, die auf die Änderung einer einzelnen Base zurückgehen können und dennoch eine große Wirkung entfalten.“
Bundesamt für Naturschutz: Hintergrundpapier zu Neuen Techniken (12.07.2017)
Bundesamt für Naturschutz: Biosafety Considerations for Plants developed by Genome Editing and other new Genetic Modification Techniques (nGMs) (2020)
Hinzu kommt, dass Untersuchungen im Labor die Wirklichkeit nur bedingt wiedergeben. Denn die Umwelt kann die angebaute Pflanze beeinflusssen und über die Epigenetik deren Genaktivitäten – auch in nachfolgenden Generationen. So können bei den Nachkommen gentechnisch veränderter Organismen neue Eigenschaften auftreten, die in der Elterngeneration nicht beobachtet wurden.
Andreas Bauer-Panskus et. al.: Risk assessment of genetically engineered plants that can persist and propagate in the environment (Environmental Sciences Europe ( 27.02.2020)
Aus all diesen Gründen fordern agro-gentechnikkritische Institutionen wie Testbiotech eine umfassende Technikfolgenabschätzung für genom-editierte Pflanzen.
Testbiotech: Agro-Gentechnik - zwischen hohen Erwartungen und komplexen Risiken (März 2023)
Regeln für CRISPR

Bisher werden in den USA und Kanada nur wenige Pflanzen angebaut, deren Erbgut mit älteren Gen-Scheren wie TALEN oder ODM verändert wurde. Dazu zählen ein herbizidtoleranter Raps der Firma Cibus oder eine in ihrem Fettsäuremuster veränderte Sojabohne der Firma Calyxt. Die meisten mit CRISPR/Cas veränderten Pflanzen befinden sich noch im Laborstadium. Vor der Markteinführung steht ein Speisepilz, der nach dem Einschneiden nicht braun anläuft sondern länger frisch aussieht. Die Pilze und mehrere andere Pflanzen wurden in den USA bereits dereguliert. Das heißt, sie dürfen ohne weitere staatliche Überprüfung angebaut werden, sobald sie fertig entwickelt sind.
Für die EU hat der Europäische Gerichtshof (EuGH) im Juli 2018 entschieden, dass Organismen, die mit Hilfe neuer gentechnischer Verfahren hergestellt wurden, unter das EU-Gentechnikrecht fallen. Sie müssen nach dessen Regeln überprüft, zugelassen und gekennzeichnet werden. Nur so lassen sich auch die Rückverfolgbarkeit der Organismen und die Wahlfreiheit der Verbraucher gewährleisten.
Das Urteil des EuGH zur Einordnung der neuen Gentechnik vom 25.7.2018
Seither fordern interessierte Wissenschaftler und Wirtschaftskreise, das EU-Gentechnikrecht zu ändern und mit CRISPR hergestellte Organismen auszunehmen, soweit kein artfremdes Erbgut eingeführt wurde. Sie begründen dies damit, dass das langwierige Zulassungsprozedere viel Geld und Zeit koste, den Züchtungsfortschritt behindere und EU-Unternehmen dadurch ausgebremst würden. Außerdem seien die vorgenommenen Änderungen nicht nachweisbar, weil sie auch durch natürliche Mutationen entstehen könnten. Ein Beispiel dafür: Max-Planck-Gesellschaft: Wissenschaftler fordern Modernisierung des europäischen Gentechnik-Gesetzes (25.07.2019)
Dem widersprechen Umwelt- und Verbraucherorganisationen ebenso wie kritische Wissenschaftler, Ethiker und Juristen. Sie argumentieren – ebenso wie die Richter des EuGH – mit dem in den EU-Verträgen verankertem Vorsorgeprinzip. Dieses verpflichte die EU dazu, die mit einer neuen Technik verbundenen Risiken zu prüfen. Auch ließen sich die neuen Methoden nachweisen, da der gentechnische Eingriff Spuren im Erbgut hinterlasse. Es fehle lediglich der politische Wille, schnell anwendungsreife Nachweisverfahren zu entwickeln. Wichtige Verbesserungen, wie zum Beispiel Widerstandsfähigkeit gegen Dürren oder Krankheiten könnten schon heute ganz ohne Gentechnik durch die normale Pflanzenzucht, erreicht werden. Zwei Beispiele dafür:
Heike Moldenhauer et. al.: Zukunft oder Zeitbombe? ( Juni 2019)
Positionspapier von rund 100 Verbänden zu den Kommissionsplänen: Gentechnik auch in Zukunft strikt regulieren (April 2022)
Die EU-Kommission und einige Mitgliedsstaaten wollen das EU- Gentechnikrecht ändern und die meisten Erzeugnisse neuer gentechnischer Verfahren von der Zulassung ausnehmen. Den Prozess dafür hat die Kommisision im April 2021 mit einem Bericht eröffnet. Zum Kommissionsbericht. Am 5. Juli 2023 legte die Kommission ihren Vorschlag für den rechtlichen Umgang mit neuen gentechnischen Verfahren (NGT) vor. Derzeit (November 2023) wird der Vorschlag mit viel Zeitdruck im Europaparlament und im Ministerrat behandelt, mit dem Ziel, die Kompromissverhandlungen im Trilog rechtzeitig vor der Europawahl im Juni 2024 abzuschließen. Das Fallbeispiel Neues Recht für Neue Gentechnik? beschreibt ausführlich dieses laufende europarechtliche Gesetzgebungsverfahren und wie die Lobbyisten der Gentechnik-Konzerne es beeinflussen.
CRISPR und das große Geld

Lebewesen, ihre Gene und die Vorgänge in ihrem Körper sind keine menschlichen Erfindungen. Auch CRISPR stammt aus der Natur, nämlich von Bakterien, die sich damit vor Feinden schützen. Dennoch haben sich die Wissenschaftler, die aus CRISPR ein gentechnisches Verfahren machten, diese Methode und ihre Anwendungen patentieren lassen. Weil diese Patente Milliarden Euro wert sind, tobte darüber ein jahrelanger Gerichtsstreit. Er wurde 2018 für die USA entschieden. In Europa beharken sich die beiden Parteien, die University of Berkeley in Kalifornien und das Broad Institut in Cambridge, weiterhin.
Die großen Saatgutkonzerne wie Bayer oder Corteva, die auch mit herkömmlichen Gentechnik-Pflanzen viel Geld verdienen, haben sich von den CRISPR - Entwicklern Lizenzen gekauft, um deren Technik nutzen zu können. Die damit hergestellten gentechnisch veränderten Pflanzen melden sie dann selbst zum Patent an. Corteva hat weltweit bereits 1.430 Patente auf Pflanzen eingereicht, die mit neuen gentechnischen Verfahren hergestellt wurden. Auf Platz zwei liegt Bayer mit 119 Patenten. Selbst der Deutsche Bauernverband und der Verband der Pflanzenzüchter warnen vor diesen Patenten, obwohl sie die neue Gentechnik befürworten. Für die Landwirte bedeutet das, dass CRISPR-Pflanzen und Tiere dem Patentschutz unterliegen und eine Nachzucht entweder verboten oder zumindest lizenzpflichtig wäre. Wobei die Konzerne erst einmal nachweisen müssten, dass es sich tatsächlich um die von ihnen entwickelten Pflanzen handelt und nicht um natürliche Mutationen. Das spricht dafür, dass es, sobald CRISPR-Pflanzen kommerziell angebaut werden, zumindest die Hersteller auch eine Nachweismethode dafür haben werden.
Infodienst: Neue Gentechnik - Biopatente bedrohen Züchtungsfreiheit (19.05.2023)
Infodienst: Bericht - Corteva meldet 1400 Patente für genomeditierte Pflanzen an (22.10.2022)
Zuletzt aktualisiert: November 2023